Take home message
Koeien kunnen genetisch verschillen in de eigenschap om A1 of A2 te kunnen vormen. Dit bepaalt de aanwezigheid van de peptide beta-casomorphine (BCM7), een mogelijk ongewenste peptide in koemelk. Concentraties in rauwe melk verschillen echter nauwelijks, maar na simulatie van de eiwitvertering met verteringssappen / enzymen zijn er grote verschillen in concentraties van BCM7.
Rauwe en verhitte melk
Beta-casomorphines (BCM) zijn peptiden die bij de afbraak van het eiwit beta-caseine kunnen ontstaan. Hoe hoog is de concentratie in melk? In laboratorium onderzoek werd het verschil in BCM7 concentratie tussen rauwe en gehydrolyseerde melk van koeien met een verschillend genotype voor A1 of A2 bepaald (Cieślińska et al., 2007). Koeien waren homozygoot A1A1, dan wel A2A2. In alle rauwe melk monsters, onafhankelijk van de A1 of A2 variant werden slechts sporen van BCM7 gevonden. Na hydrolyse van de melk met behulp van het eiwit pepsine in een zure omgeving valt het melkeiwit uiteen in brokstukken. Pepsine bevindt zich in de maag en maakt onderdeel uit van de spijsvertering (eiwitsplitsing). Na de pepsinebehandeling zijn er verschillen in BCM7 concentraties in A1 en de A2 melk, respectievelijk 12 en 3 ng/ml, een verviervoudiging in melk, die kunstmatig verteerd is.
Later onderzocht men (Cieślińska et al., 2012) in meer detail het effect van lactatiestadium van de koe, genotype van de koe en verhitting op het vrijmaken van BCM7 in het laboratorium (in vitro test). Daartoe werd een vergelijking gemaakt tussen: (1) rauwe melk, (2) melkpoeder, (3) hoog gepasteuriseerd (95oC, 20 min) of (4) gesteriliseerd (117oC, 5 min). Er zijn geen verschillen in BCM7 door het lactatiestadium van de koeien, hetgeen aangeeft dat we met een genetisch verankerde uitkomst te maken hebben. Net als in 2007, laten zowel de A1 als de A2 rauwe melk nauwelijks verschillen in BCM7 gehalte zien. Verschillen ontstaan, wanneer de melk in vitro wordt blootgesteld aan verteringsenzymen: (1) alleen pepsine of (2) een mix van enzymen (pepsine, trypsine en elastase). Dit laatste mengsel is een betere simulatie van hetgeen zich in het maagdarmkanaal afspeelt. In deze vitro vertering ontstaan grote verschillen tussen A1A1 en A2A2 melk. Met pepsine alleen neemt de vrijgemaakte BCM7 met een factor 7 toe ten opzichte van de rauwe melk en met het hele enzympakket zelfs een factor 200. De homozygote A2A2 melk geeft in vitro een geringere toename, respectievelijk 5 en 27x dan de A1A1 melk (Figuur 1). Er is geen verschil tussen de vormen van hittebehandeling en de uitkomsten die men hier vindt zijn van dezelfde orde van grootte als in figuur 1.
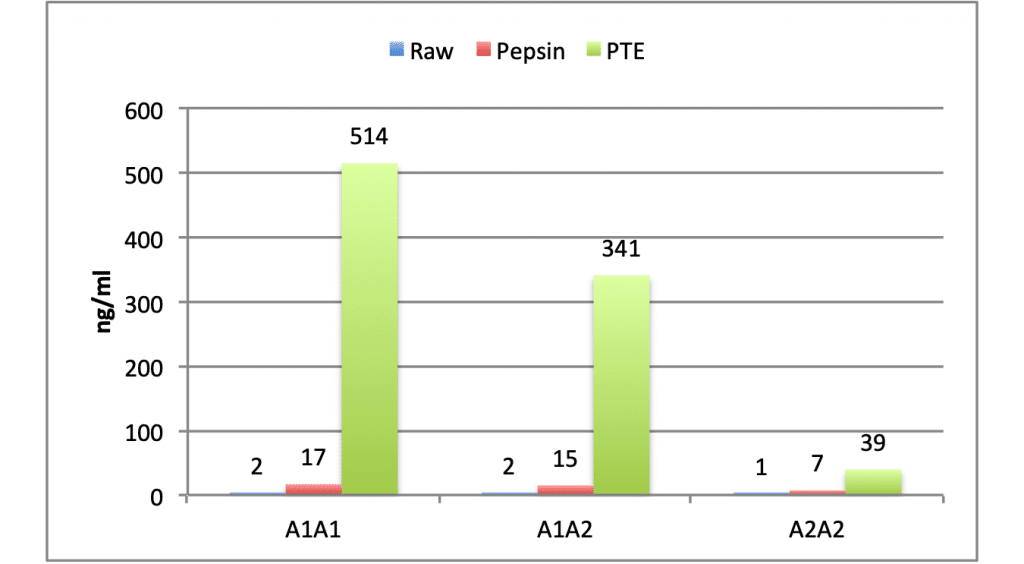
Dergelijk in vitro onderzoek wijst de A1 melk aan als de bron van de BCM7-problematiek. Dat er ook sporen BCM7 in A2A2 melk wordt gevonden wijt men aan de monstervoorbereiding en de lage pH die in vitro wordt gekozen. Met name de genetica van de koeien zorgt voor de potentiele verschillen en niet zozeer de hittebehandeling, is de voorlopige conclusie.
Literatuur
- Cieślińska, A., Kamiński, S., Kostyra, E., & Sienkiewicz-Szłapka, E. (2007). Beta-casomorphin 7 in raw and hydrolyzed milk derived from cows of alternative β-casein genotypes. Milchwissenschaft, 62(2), 125-127.
- Cieślińska, A., Kostyra, E., Kostyra, H., Oleński, K., Fiedorowicz, E., & Kamiński, S. (2012). Milk from cows of different β-casein genotypes as a source of β-casomorphin-7. International journal of food sciences and nutrition, 63(4), 426-430.
Foto: geiten en schapen produceren melk met een A2 samenstelling




